科研进展
WHO:严重急性呼吸道感染临床照护——第五章丨急性呼吸道感染的鉴别诊断
WHO:Clinical Care for Severe Acute Respiratory Infection
WHO:严重急性呼吸道感染临床照护
山东大学齐鲁医院急诊科
山东省医学会急诊医学分会/护理学组
第五章 急性呼吸道感染的鉴别诊断
总结
SARI的鉴别诊断包括广谱的社区获得性病原体、呼吸道病毒、细菌以及一些少见的微生物。鉴别诊断的优先顺序将根据宿主因素(例如年龄、是否患有慢性疾病、旅居史、接种疫苗)、环境因素(如地理位置、病媒等)、当地流行病学(如病原体在社区的流行程度、地方性感染)和病原体因素(如嗜肺性)而异。详情参见第1章。应当根据鉴别诊断和临床前期试验结果的可能性选择不同的诊断检测方法。
对于有急性上呼吸道感染症状的患者,建议采集上呼吸道样本以指导进一步治疗。应尽快进行检测以指导治疗计划的制定。采集标本时采取适当的IPC感染预防措施。参考疑似或确诊冠状病毒疾病(COVID- 19)的医疗保健期间的感染预防和控制(https://www.who.int/publications/i/item/WHO-2019-nCoV-IPC-2021.1)
首选采集患者的上呼吸道标本(上呼吸道:鼻咽和口咽),如果仍存在临床疑似病例且上呼吸道标本为阴性,则在有条件的情况下采集下呼吸道标本(下呼吸道:痰液、机械通气患者的气管内吸出物或支气管肺泡灌洗物),通过RT-PCR或抗原快速诊断检测和细菌染色/培养进行SARS-CoV-2检测。
如果患者出现符合SARI标准的体征或症状,还应收集:
• 血液和痰液样本应进行细菌培养,以判断引起肺炎和脓毒症的潜在细菌性病因,最好是在抗微生物治疗之前进行。但是即使没有进行细菌培养或尚未获得培养结果,也不应延迟经验性和适当的抗微生物治疗。
对于流行病感染地区应参考当地实际情况采取相应措施:
• 在疟疾流行地区,发热患者应接受疟疾检测并得到适当治疗。
• 在虫媒病毒感染流行的地区,可考虑对未分化发热性疾病患者进行登革热、基孔肯雅热或黄热病检测,特别是出现血小板减少的情况时。
• 在结核病高发地区,应当考虑进行结核病检测。
• 登革热流行地区可能并发SARS-CoV-2感染,因此,登革热诊断检测呈阳性时也仍需开展COVID-19检测。
参考世卫组织SARS-CoV-2感染诊断检测(https://www.who.int/multi-media/details/diagnostic-testing-for-sars-cov-2-infection)(https://www.who.int/publications/i/item/diagnostic-testing-for-sars-cov-2)
参考世卫组织结核病指南:最新更新(https://www.who.int/publications/digital/
global-tuberculosis-report-2021/featured-topics/tb-guidelines)。
参考世卫组织疟疾检测(https://www.who.int/teams/global-malaria-programme
/case-management/diagnosis)。
工具
5.1 SARS-CoV-2感染诊断检测
5.2 应用SARS-CoV-2抗原检测快速诊断检测
5.3 上呼吸道标本采集试剂盒
5.3.1 鼻咽拭子技术
5.3.2 咽后拭子或咽拭子技术
5.3.3 气管抽吸技术
5.4 标本保存指南
5.5 标本运输材料
5.6 标本运输指南
5.7 SARI患者血液培养采集指南
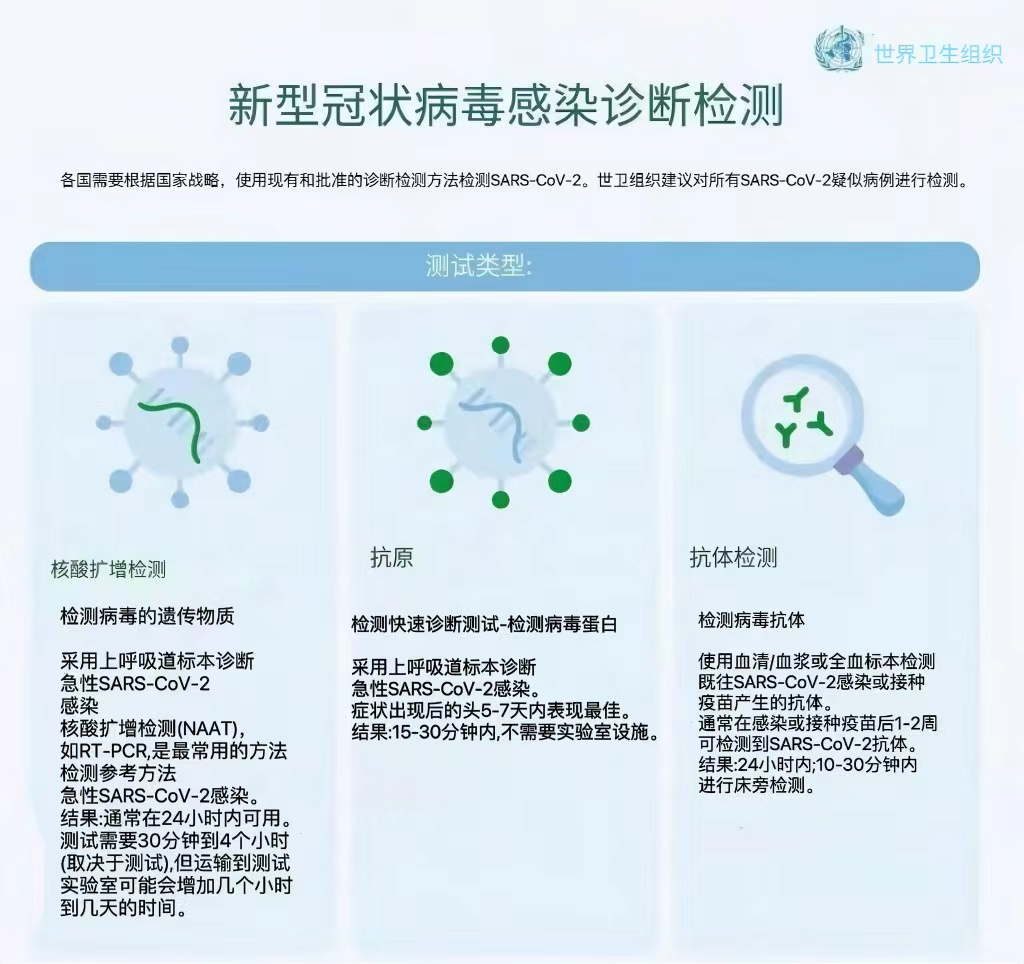
有关进一步信息,请参阅世卫组织SARS-CoV-2感染诊断检测和COVID-19检测视频
(https://www.who.int/multi-media/details/diagnostic-testing-for-sars-cov-2-infection)
(https://www.youtube.com/watch?v=PhdSdJu_QXI)
5.2 应用SARS-CoV-2抗原检测快速诊断检测
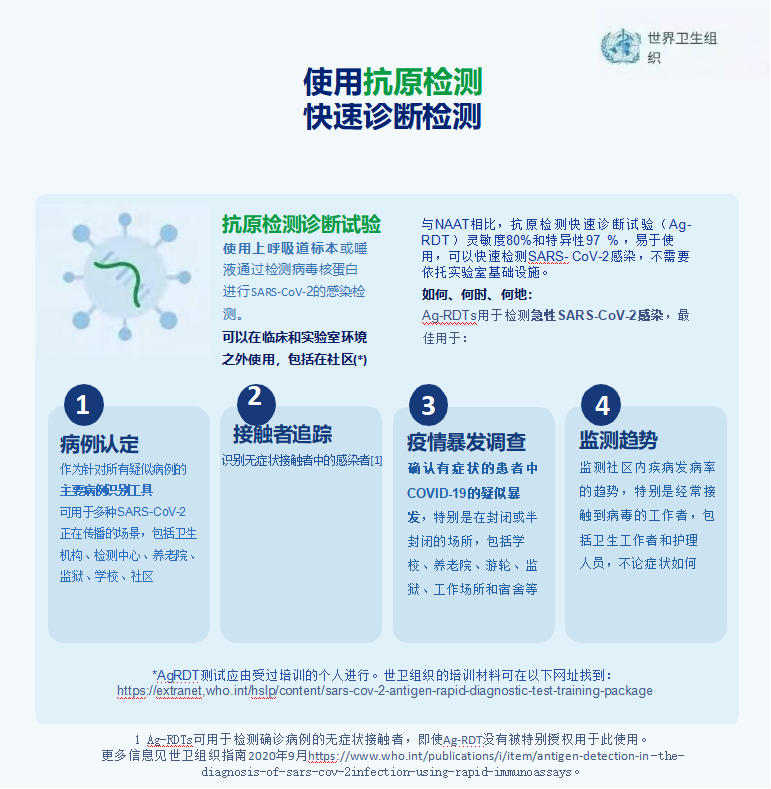
在诊断SARS-CoV-2感染方面,详情见世卫组织使用抗原检测、快速诊断检测和抗原检测
(https://www.who.int/multi-media/details/use-of-antigen-detection-rapid-diagnostic-testing)
(https://www.who.int/publications/i/item/antigen-detection-in-the-diagnosis-of-sars-cov-2infection-using-rapid-immunoassays)
在开始采集标本之前,最好先准备一个标本收集工具包。这是URT标本收集工具包中应该包含的所有项目的清单。
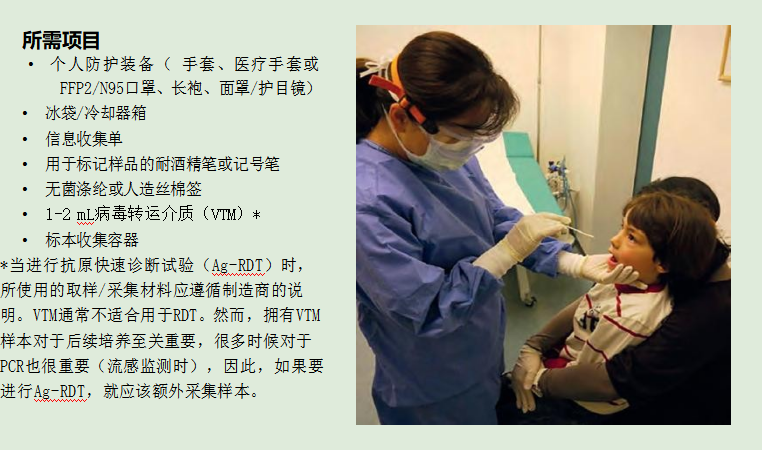
1. 消毒采样管。
2. 使用柄部为刚性(塑料)材料的拭子进行咽喉和鼻腔采样的标本。
3. 使用压舌板进行咽拭子采样。
4. 使用无菌生理盐水(0.9%氯化钠)进行鼻咽抽吸物时。
5. 使用痰液或粘液收集器进行鼻咽抽吸(需负压)。

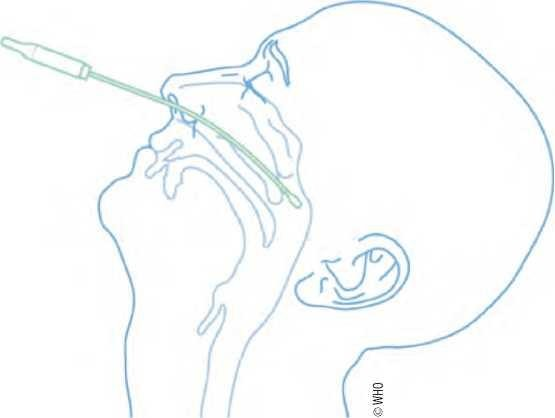
5.3.1 鼻咽拭子技术

技术
1. 采用标准、接触和飞沫预防措施。
2. 将拭子插入一个鼻孔,再回到鼻咽。
3. 将拭子原地放置几秒钟。
4. 然后慢慢取出拭子,同时旋转到鼻咽后表面。
5. 取出拭子;插入带有VTM的采样管或容器中。
6. 标记采样管或样本容器。
7.采集后,立即将标本运送到实验室进行病毒PCR检测和/或病毒抗原检测。如果不能及时运送到实验室,请将标本置于冰上或进行冷藏。
婴幼儿鼻咽拭子:
• 使用适当大小的拭子:测量从鼻子到耳朵(人中到耳屏)的距离。
• 插入一半或整个拭子,当遇到阻力时停止。
• 将拭子水平插入,插入下鼻甲下方,而不是斜插入鼻头上方。
如何采集口咽和鼻咽标本诊断COVID-19 ( https://www.youtube.com/watch?v=jh6Is9oPyyw)。
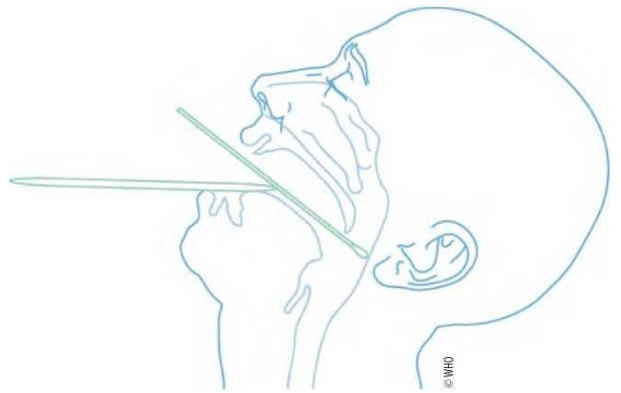
5.3.2 后咽拭子或咽拭子技术

技术
1. 采用标准、接触和飞沫预防措施。
2. 让受试者尝试张开嘴,说“啊”来抬高悬雍垂。
3. 用压舌板压舌。
4. 用拭子擦拭后咽,不要用拭子接触舌头。
5. 插入带有VTM的采样管或容器中。折断拭子头部,确保采样管或容器能够闭合。
6. 标记采样管或容器。
7. 立即将标本运送到实验室进行病毒PCR检测和/或病毒抗原检测。如果不能及时送往实验室,将标本置于冰上或冷藏。
有关进一步信息,请参见鼻中鼻甲和鼻咽拭子的最佳插入深度和收集口咽和鼻咽标本以诊断
COVID-19的视频
(https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8306705/pdf/diagnostics-11-01257.pdf)
(https://www.youtube.com/watch?v=cY2YKm_nel0)
5.3.3 气管内吸引技术
适用于已插管和接受有创机械通气(IMV)的患者。

1. 采用标准、接触、飞沫和空气传播的预防措施。
2. 患者准备:使用100%吸入氧气(FiO2)预加氧,给予足够的镇静。
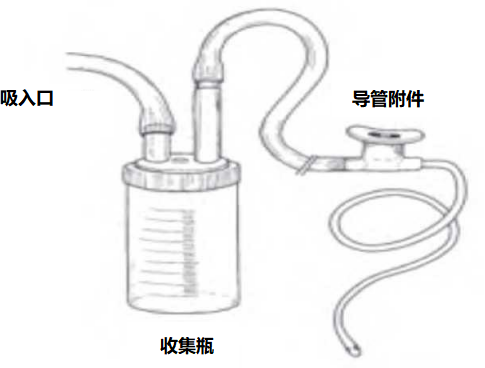
3. 将痰液取样器连接到导管和吸入出口上,打开吸力装置以确保其能正常工作,然后关闭它。
4. 准备好后,从气管导管上断开呼吸机管。
5. 在不进行抽吸的情况下,将无菌吸引导管装置插入气管导管,距尖端约2-3cm。
6. 打开吸力并收集样本进入痰液取样器,保持收集瓶直立,以防止分泌物进入泵内。缓慢取出导管,更换吸气管。
7. 如样本量不足,灌注3-5 mL无菌生理盐水,两次充气/深呼吸后抽吸。
8. 采集后立即将标本送往实验室进行病毒检测和细菌学检测。
9. 在冰箱(2-8°C)中最多保存24小时。
10.如果不能及时送检,< -20°C冰箱内保存。
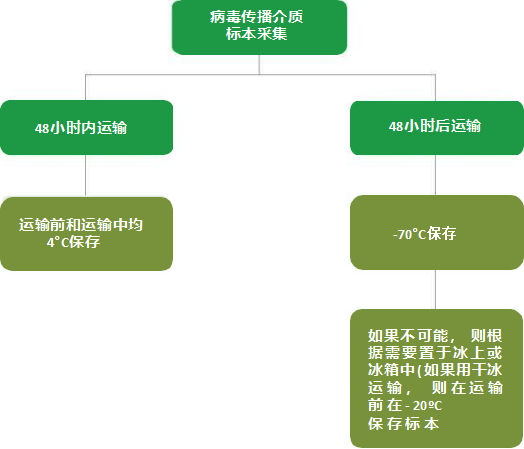
采样后立即使用病毒转运介质进行病毒分离和检测,转运介质可以防止标本变干、防止细菌和真菌生长。
虽然你应该尽快将VTM的标本送到实验室,但如果这么做有困难,把标本送到实验室之前,恰当保存非常重要。

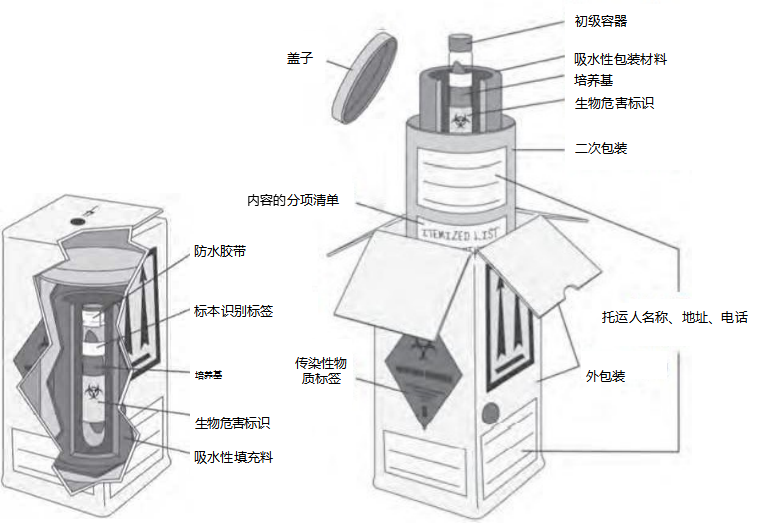
5.5 标本运输材料
打包标本时,盛放容器中不应超过500毫升。从采样现场到实验室运输时,必须使用三层包装,以保护标本在运输过程中不被破坏。

未经冷藏的传染性物质的包装和标签
SARS-CoV-2标本应归为A类、UN2814、“传染性物质,感染人类”。临床样品将被归类为UN3373、“生物物质类B” 。
• 与冠状病毒疾病(COVID-19)相关的实验室生物安全指南(https://www.who.int/ publications/i/item/laboratory-biosafety-guidance-related-to-coronavirus-disease- (covid-19))
《2021-2022年传染性物质运输法规指南》(https://www.who.int/publications/i/item/ 9789240019720)

5.7 SARI患者血液培养采集指南
医院内所有脓毒症患者在开始抗菌治疗前均应进行血培养。幸存脓毒症治疗指南(Surviving Sepsis Campaign guidelines)警告,抗菌素治疗不能因为等待血培养或血培养结果而延误超过45分钟。
该技术改编自美国疾病控制和预防中心(CDC)网站(https://www.cdc.gov/antibiotic-
use/index.html?CDC_AA_refVal=https%3A%2F%2Fwww.cdc.gov%2Fantibiotic-use% 2Fhealthcare%2Findex.html)

技术
1. 核查患者身份,解释操作过程。
2. 洗手。
3. 用70%异丙醇(酒精垫)圆形消毒瓶盖,待干。
4. 用洗必泰(消毒)棉棒消毒穿刺部位。应用无菌技术,从无菌包中取出棉棒。向下握住并按压,消毒液释出。在干燥的皮肤上来回涂抹30秒。待干。
5. 用无菌针穿刺静脉。如果在穿刺部位消毒后需要触摸静脉,请佩戴无菌手套。
6. 成人收集10-20ml;对于儿童,每组血培养取3-5mL。
7. 拔出针头,将血液分到两个血培养瓶,将穿刺针头垂直置入瓶中。培养瓶不能太满。如果两瓶血液都不够,最好将需氧瓶装满。有一些装置带的血培养瓶可以直接抽取血液,如果有这样的装置,最好采用它来采血。
8. 轻轻旋转瓶子,混合血液和液体培养基。
9. 每次脓毒症发作进行两次血培养(单独采集)就可以(心内膜炎除外)。
10.贴好标签,放入密封袋,送实验室。

致谢
感谢山东大学护理与康复学院崔乃雪教授提供专家意见。
世界卫生组织《Clinical care of severe acute respiratory infections – Tool kit》,翻译不是由世界卫生组织(世卫组织)进行的。世卫组织不对本翻译的内容或准确性负责。英文原版为装订版和正版。
https://www.who.int/publications/i/item/clinical-care-of-severe-acute-respiratory-infections-tool-kit
编辑丨国康
审核丨张敏 边圆 徐峰
